

研究開発
RESEARCH AND DEVELOPMENT
研究開発


RESEARCH AND DEVELOPMENT
ウイルスは、感染した細胞の中で増殖するときに、その細胞で発現しているさまざまな因子(宿主因子)を利用する。キノファーマでは、このウイルスが利用する宿主因子をターゲットとしウイルスの増殖を抑制する新しいコンセプトの抗ウイルス薬開発に取組んでいます。ウイルスの持つ因子に作用する従来の抗ウイルス薬とは異なるアプローチで、この取り組みにより、
この創薬戦略が実を結びつつあるのが、子宮頸がんの原因であるヒトパピローマウイルス(HPV)感染症に対する抗ウイルス薬です。HPVにはいまだに効果的な抗ウイルス薬が承認されていません。またHPVには多くの異なるタイプがあり、子宮頸がんの原因となるハイリスク型HPVには10以上のタイプがあることがわかっています。従来用いられてきたHPVワクチンではこのうち2タイプしか、また新たに承認された新しいHPVワクチンでも7タイプしか予防効果が認められておらず、キノファーマの抗ウイルス薬では効率よくすべてのハイリスク型HPVへの増殖抑制が可能となります。
タンパク質からなる「殻」とその内部に入っている「核酸(遺伝情報物質)」によって組成される、シンプルな微小構造体で、他の生物(宿主)に感染し、宿主細胞の持つ増殖機構を利用することにより自己複製します。ウイルスの自己複製により、宿主細胞が細胞死に至ったり、感染細胞ががん化することなどがあり、加えて複製された大量のウイルスへの宿主の防御機構などによる生理反応により、様々な病気を惹き起こします。
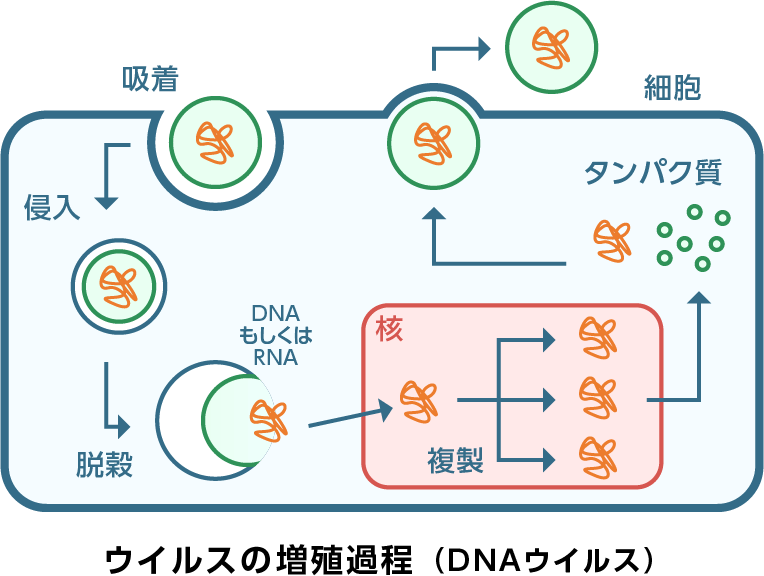

ウイルスを大きく2種に分類すると、B型肝炎や子宮頸がんに代表される疾患の原因となるDNAウイルスとインフルエンザやC型肝炎に代表される疾患の原因となるRNAウイルスに分けられます。
当社は、ウイルスが増殖時に必要なヒト宿主因子をターゲットとする新しいコンセプトで、両分類(RNAウイルス、DNAウイルス)それぞれに対する抗ウイルス薬プログラムを推進しております。
ウイルスの種類(ボルティモア分類)

DNAウイルスは多種多様な疾病を引き起こす原因となりますが、未だに有効な薬剤のない疾患も多く、この深刻なアンメットニーズに応えるべく開発に注力しています。
キノファーマの抗DNAウイルス薬は、ウイルスが複製・増殖時に利用する宿主の酵素を阻害し複製活動を抑止することで、ウイルスの増殖を抑えます。
子宮頸部上皮内腫瘍(子宮頸がん前がん病態)
疣贅(ゆうぜい、皮膚のイボ)
尖圭コンジローマ(性器、肛門周囲のいぼ)
RNAウイルスとは、ゲノムとしてRNAを持つウイルスです。ウイルスRNAの複製時には、DNA複製時にある複製エラーをチェックする機構が働かないため、突然変異を起こしやすい特徴を持っています。ヒトに加えコウモリ、豚、トリなどに存在するウイルスが異種間あるいは同種間で他の宿主に伝搬する際にも突然変異のリスクが高まります。また、ウイルス蛋白を直接的に標的とした従来の抗ウイルス薬では、投与により一定の確率で突然変異が起こり、その抗ウイルス薬に対する薬剤耐性ウイルス発生のリスクが伴うことが知られている。キノファーマでは、複数のRNAウイルスに共通する、増殖に必要なメカニズムを担う宿主因子をターゲットにすることにより、ウイルスの突然変異による薬剤耐性が起こりにくく、且つ広範なRNAウイルスに対して効果を有する新規治療薬開発を進めています。
コロナウイルスなどの一本鎖RNAウイルスは、宿主細胞の遺伝子とは異なり、細胞質のみでウイルス遺伝子の複製・発現が制御されています。即ち、ウイルスRNAの複製やウイルス粒子の構築といった、非感染細胞では存在しない複雑な過程を経て増殖します。成熟ウイルスを効率よく産生するために、一本鎖RNAウイルスは感染初期の段階で細胞質内にウイルス複製の場を構築することが明らかになりつつあります。キノファーマでは独自のコンセプトとして、成熟ウイルス粒子を生産させない、ウイルス複製の場を阻害する抗ウイルス剤、即ち「ウイルス生産工場阻害剤」の研究開発を推進しています。得られた阻害剤は、新型コロナウイルス(SARS-Cov-2)のみならず、今後も発生のリスクが想定されるRNAウイルスによるパンデミックに対しても適応可能と考えられます。
ダウン症は、体細胞の21番染色体が通常より1本多い計3本(トリソミー)、あるいは少数ですが、21番染色体の一部がトリソミーになることで発症する先天性疾患です。症状としては、身体的発達の遅延、特徴的な顔つき、軽度の知的障害が特徴であるが、40歳以降にアルツハイマー病が高確率で起きることが知られている。
キノファーマは、この21番染色体上にあり、様々なトリソミーの解析からダウン症責任領域(Down syndrome critical region)にあるDyrk1a遺伝子を標的とする神経変性疾患治療薬を開発しています。
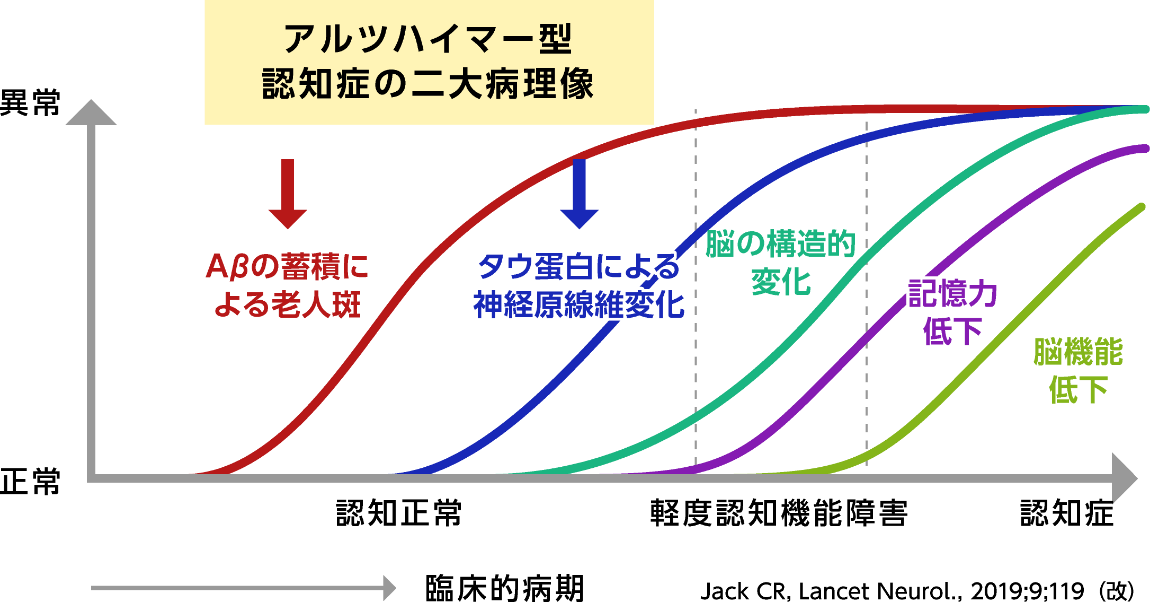
アルツハイマー病の根本原因は解明されておらず、複数のアプローチからの研究開発が行われています。 原因がアミロイドβ(Aβ)の凝集・沈着であるという仮説に基づき、多くの「Aβ標的薬」が開発されております。臨床試験では、認知機能の改善は想定されたほどではなく、開発中止となる候補医薬品も出てきています。
そのような中で過剰リン酸化タウの細胞内凝集体の「神経原線維変化」が実際の神経細胞脱落と相関することが判明し、タウ蛋白がアルツハイマー病治療薬の対象として注目されてきています。
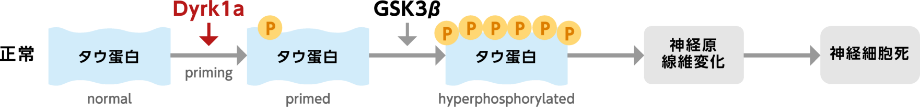
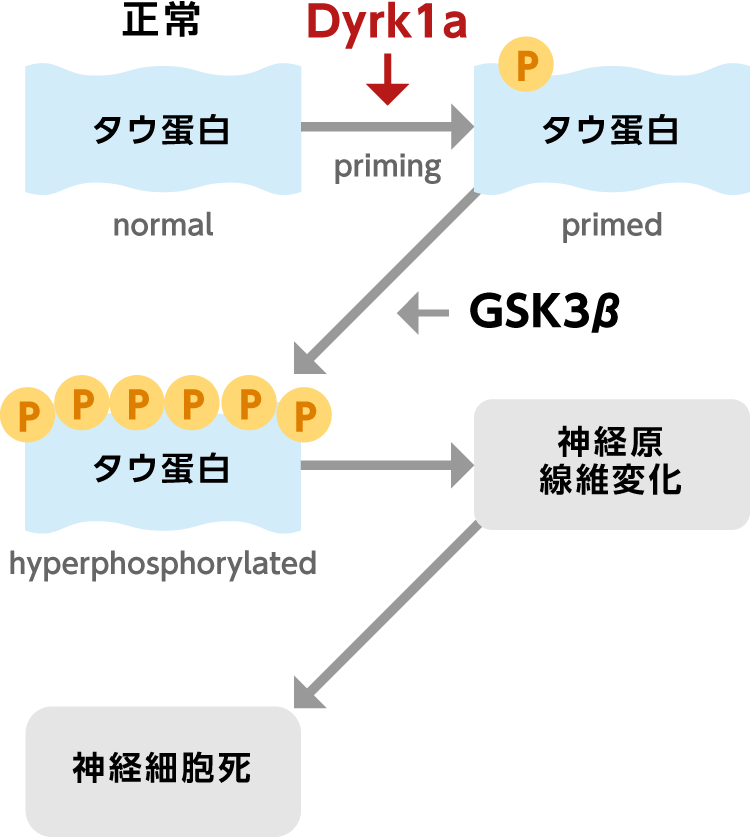
タウ蛋白はまず、キナーゼの一種である「Dyrk1a酵素」によりリン酸化され、その後過剰なリン酸化が生じて、タウ蛋白の凝集の引き金に繋がるとなると考えられています。 当社候補化合物は、「Dyrk1a酵素」を阻害する効果を有していることから、アルツハイマー病の発現予防や進展防止効果を示すと考えています。
スペインの研究チームにより、緑茶抽出成分(Dyrk1a阻害能を有する)がダウン症患者の認知機能を改善するという第2相臨床試験による研究成果が発表されています。キノファーマでは、より高い阻害能を有する当社候補化合物によりダウン症およびアルツハイマー病に対する臨床試験を計画しています。